随着2025版《美国临床内分泌学会(AACE)成人血脂异常管理指南》的发布,低密度脂蛋白胆固醇(LDL-C)目标值再次刷新!
LDL-C降到多少,斑块才能稳定不破裂?他汀、PCSK9抑制剂怎么选?哪些人必须终身用药?
55岁的刘先生因LDL-C超标未干预,突发心梗抢救,今天我们从最新指南和真实病例出发,说清血脂管理的生死红线!

2025版AACE指南核心更新
1 LDL-C目标值分层更严格
2025版AACE指南对LDL-C(低密度脂蛋白胆固醇)目标值进行了更为严格的分层,以更好地指导临床实践,降低心血管事件风险。具体分层如下:
1.极端高危患者(如心梗复发、多支血管病变)
LDL-C目标值 <1.0 mmol/L。
这是本次指南的突破性调整,强调了对此类患者更严格的血脂控制,以最大程度降低再发事件的风险。
2.极高危患者(如糖尿病合并肾病)
LDL-C目标值 <1.4 mmol/L。
糖尿病和肾病的并存显著增加了心血管风险,因此需要更积极的降脂治疗。
3.高危患者(如高血压+吸烟)
LDL-C目标值 <1.8 mmol/L。
高血压和吸烟是心血管疾病的独立危险因素,联合存在时需强化血脂管理。
4.中危患者
LDL-C目标值 <2.6 mmol/L。
对于中危患者,目标值相对宽松,但仍需积极干预以预防心血管事件。
2 新增风险评估工具
为了更好地识别和管理心血管高危人群,2025版AACE指南引入了新的风险评估工具:
1.Lp(a) ≥50 mg/dL:直接列为高危人群
脂蛋白(a) [Lp(a)] 是独立的心血管危险因素,高水平的Lp(a)与动脉粥样硬化性心血管疾病(ASCVD)风险显著相关。指南建议对所有患者进行Lp(a)检测,并将Lp(a) ≥50 mg/dL者直接归为高危人群,需强化降脂治疗。
2.冠状动脉钙化积分(CAC):用于中危患者的风险再分层
CAC是评估冠状动脉粥样硬化程度的有效工具,尤其适用于中危患者的风险评估。CAC积分高者(如≥100 Agatston单位)可升级为高危,需更积极的干预措施。
3药物推荐升级
2025版AACE指南对降脂药物的推荐进行了重要调整,特别是PCSK9抑制剂的地位提升:二线治疗升至一线治疗(与他汀联用)。
PCSK9抑制剂(如依洛尤单抗、阿利西尤单抗)在降低LDL-C方面效果显著,尤其适用于他汀类药物无法达标或不能耐受的患者。新版指南建议,对于极端高危和极高危患者,可直接启动他汀与PCSK9抑制剂的联合治疗,以快速达标。
LDL-C降到多少才能稳住斑块?
1 极端高危患者:LDL-C <1.0 mmol/L
目标人群:
- 复发性ASCVD患者:在2年内多次发生动脉粥样硬化性心血管疾病(如心梗、脑梗)。
- 冠状动脉多支病变患者:冠状动脉存在多处狭窄,且狭窄程度≥50%。
研究支持:
- 《新英格兰医学杂志》:研究表明,将LDL-C控制在<1.0 mmol/L时,斑块的脂质核心可缩小40%,从而显著降低斑块的不稳定性,减少心血管事件的发生。
临床意义:
对于极端高危患者,强化降脂治疗是必要的。通过将LDL-C降至<1.0 mmol/L,可以有效逆转斑块进展,降低斑块破裂风险,从而减少心梗、脑梗等严重事件的发生。
2 极高危患者:LDL-C <1.4 mmol/L
目标人群:
- 糖尿病合并慢性肾病患者:糖尿病患者同时伴有慢性肾病,且肾小球滤过率(eGFR)<60 mL/min/1.73m²。
- 家族性高胆固醇血症患者:LDL-C水平显著升高(≥4.9 mmol/L),且具有家族遗传史。
研究支持:
- 《美国心脏病学会杂志》:数据显示,LDL-C每降低1 mmol/L,斑块破裂的风险可降低28%。对于极高危患者,将LDL-C控制在<1.4 mmol/L可显著降低心血管事件的发生率。
临床意义:
极高危患者通常具有多重危险因素,因此需要更严格的LDL-C控制目标。通过将LDL-C降至<1.4 mmol/L,可以有效降低斑块破裂风险,延缓疾病进展。
3 高危患者:LDL-C <1.8 mmol/L
目标人群:
- 高血压合并肥胖患者:高血压患者同时伴有肥胖(BMI≥30)。
- 10年ASCVD高风险患者:根据风险评估模型,10年内发生动脉粥样硬化性心血管疾病的风险≥20%。
研究支持:
- 《柳叶刀》:研究表明,将LDL-C控制在<1.8 mmol/L时,斑块的钙化稳定性可提升50%,从而降低斑块破裂的风险。
临床意义:
对于高危患者,将LDL-C控制在<1.8 mmol/L是基本目标。这一目标可以有效稳定斑块,减少心血管事件的发生,同时为患者提供更好的长期预后。
如何用药?指南推荐的4大方案
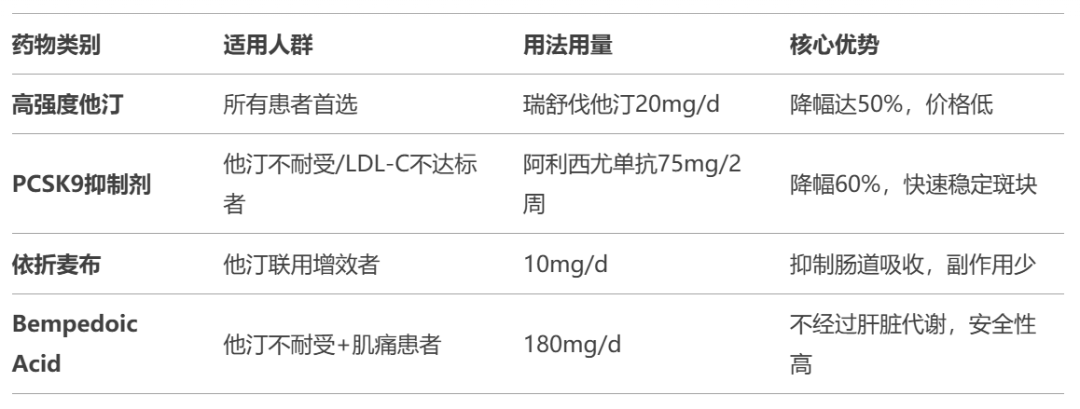
他汀类药物作为降脂治疗的首选药物,具有显著的降脂效果和经济的用药成本,成为控制低密度脂蛋白、减少心血管风险的重要药物。在众多他汀类药物中,第三代强效品种如阿托伐他汀、瑞舒伐他汀等,能有效降低LDL-C水平30%-50%。PCSK9抑制剂类药物的普及,为极高心血管风险及对他汀类药物不耐受的患者提供了更有效的新手段。
PCSK9抑制剂的常规用法是与第三代他汀类药物联用,针对极高风险患者加强低密度脂蛋白的控制,或者单独用于对他汀类药物完全不耐受的高风险患者。依折麦布通过抑制肠道胆固醇吸收,与他汀类药物并用能进一步增加降脂效果。
最新指南还推荐了新近批准的口服降脂药贝派地酸,对于不适合使用他汀类药物的患者,它展现出了良好的替代效果。专家指出,降脂治疗的重点应放在“稳定达标”而非单纯的“数值高低”上。患者应在医生的专业指导下,依据个人状况制定个性化的治疗方案,避免盲目追求极端的指标数值。
真实案例:刘先生的生死教训
初始情况
刘先生,45岁,公司高管,平时工作繁忙,压力大,生活节奏快。在一次例行体检中,发现他的低密度脂蛋白胆固醇(LDL-C)高达4.8mmol/L,远高于正常值(正常应小于3.0mmol/L)。进一步的冠状动脉造影显示,他的冠状动脉狭窄达到40%,这意味着他的心脏供血已经受到一定程度的影响。
医生建议刘先生立即开始药物治疗,包括他汀类药物以降低胆固醇,并配合阿司匹林等抗血小板药物预防血栓形成。然而,刘先生对药物有较强的抵触心理,认为自己还年轻,身体底子好,仅通过控制饮食和加强锻炼就能解决问题。因此,他拒绝了医生的用药建议,决定“靠自己”来改善健康状况。
干预措施
刘先生开始尝试控制饮食,减少高脂肪、高胆固醇食物的摄入,但他并没有严格遵循医生的饮食建议,偶尔还是会吃一些油炸食品和红肉。此外,他虽然知道吸烟对心血管健康极为不利,但由于工作压力大,始终未能成功戒烟,每天仍然保持半包到一包的吸烟量。
在运动方面,刘先生也未能坚持。他原本计划每周至少进行三次有氧运动,如跑步或游泳,但由于工作繁忙,常常加班到深夜,运动计划逐渐被搁置。最终,他每周的运动次数不到一次,甚至有时一个月都未能进行一次有效的锻炼。
1年后突发心梗
一年后的一天,刘先生在办公室突然感到胸口剧烈疼痛,伴随冷汗和呼吸困难。同事立即拨打了急救电话,将他送往医院。急诊医生通过心电图和心肌酶谱检查,确诊为急性心肌梗死。进一步的冠状动脉造影显示,他的左前降支已经完全闭塞,这是心脏供血的主要血管之一,情况十分危急。
医生迅速为刘先生进行了介入手术,植入了两枚支架,以恢复心脏的血液供应。手术虽然成功,但刘先生的心脏已经受到了不可逆的损伤,心功能明显下降,未来发生心力衰竭的风险大大增加。
现治疗方案
经历了这次生死考验,刘先生终于意识到自己之前的错误决定有多么危险。他开始严格按照医生的建议进行治疗。目前,他的治疗方案包括:
瑞舒伐他汀20mg/d:这是一种强效的他汀类药物,能够显著降低血液中的LDL-C水平。刘先生每天坚持服用,将LDL-C从之前的4.8mmol/L降至0.8mmol/L,远低于目标值。
阿利西尤单抗:这是一种PCSK9抑制剂,能够进一步降低胆固醇水平,尤其是对于那些对他汀类药物反应不佳的患者。刘先生每两周注射一次,帮助他维持极低的LDL-C水平。
生活方式调整:刘先生彻底戒了烟,并严格控制饮食,避免高脂肪、高胆固醇的食物。他还聘请了私人教练,每周进行至少三次有氧运动,如跑步、游泳和骑自行车,以增强心肺功能。
心理辅导:由于心梗带来的心理阴影,刘先生还接受了心理辅导,帮助他缓解焦虑和压力,避免因情绪波动再次诱发心血管事件。
反思与教训
刘先生的经历是一个典型的“生死教训”。他最初的拒绝用药和不良生活习惯,最终导致了严重的心血管事件。通过这次事件,刘先生深刻认识到:
早期干预的重要性:心血管疾病是一个渐进的过程,早期发现并积极干预,可以避免病情恶化。刘先生如果在一开始就接受药物治疗,或许可以避免心梗的发生。
药物治疗的必要性:对于高胆固醇和冠状动脉狭窄的患者,药物治疗是不可或缺的。仅靠饮食和运动,往往无法达到理想的治疗效果。
生活方式的全面改善:戒烟、健康饮食和规律运动是预防心血管疾病的基础。刘先生通过这次教训,彻底改变了自己的生活方式,从而降低了未来再次发病的风险。
医生私藏的3个控脂秘诀
1 饮食控脂技巧
早餐:燕麦+奇亚籽(富含β-葡聚糖,吸附胆汁酸)。
晚餐:清蒸深海鱼(每周3次,补充EPA/DHA)。
2 运动优化方案
HIIT训练:每周3次,20分钟/次(降脂效率是匀速运动的2倍)。
抗阻运动:哑铃深蹲+弹力带(提升肌肉代谢,降低LDL-C)。
3 药物联用策略
他汀+PCSK9抑制剂:适合极端高危患者(LDL-C降幅>75%)。
他汀+依折麦布:适合经济受限者(月费用<200元)。
在低密度脂蛋白的管理过程中,患者常常会遇到一些困惑和误区。以下是三个最常见的问题及其专业解答。
Q1 LDL-C降到1.0以下会太低吗?
不会!根据最新的医学研究,低密度脂蛋白胆固醇(LDL-C)降到1.0mmol/L以下不仅安全,而且对心血管高危患者(如冠心病、心梗、糖尿病等)非常有益。美国临床内分泌医师协会(AACE)指南明确指出,LDL-C低至0.5mmol/L仍然是安全的,且能够显著降低心血管事件的风险。
多项大型临床试验(如FOURIER、ODYSSEY OUTCOMES)表明,极低的LDL-C水平(<1.0mmol/L)可以进一步减少动脉粥样硬化斑块的进展,甚至逆转斑块的形成。对于已经发生过心梗或植入支架的患者,将LDL-C控制在极低水平是预防复发的关键。
Q2 吃他汀后肌肉酸痛怎么办?
肌肉酸痛是他汀类药物的常见副作用之一,但并非无解!以下是两种有效的解决方案:
换用Bempedoic Acid(贝派地酸): 这是一种新型降脂药,作用机制与他汀类似,但不会引起肌肉酸痛,适合对他汀不耐受的患者。
联合辅酶Q10(200mg/d): 他汀类药物可能降低体内辅酶Q10的水平,导致肌肉酸痛。补充辅酶Q10可以缓解这一症状,同时保护肌肉细胞功能。
如果肌肉酸痛伴随肌无力或尿液颜色变深(可能提示横纹肌溶解),需立即停药并就医。切记!肌肉酸痛并不意味着必须停药,通过调整药物或补充辅酶Q10,大多数患者可以继续安全地控制血脂。
Q3 Lp(a)高怎么降?
脂蛋白(a) [Lp(a)] 是一种与遗传密切相关的血脂指标,目前尚无特效药物能够直接降低Lp(a)。但以下措施可以帮助控制其危害:
强化LDL-C控制: 虽然Lp(a)无法直接降低,但将LDL-C控制在极低水平(<1.4mmol/L)可以减少整体心血管风险。
脂蛋白血浆置换: 对于Lp(a)极高且反复发生心血管事件的高危患者,脂蛋白血浆置换是一种有效的治疗手段,可以快速降低Lp(a)水平。
新型药物研究: 目前,针对Lp(a)的药物(如Pelacarsen)正在临床试验中,未来可能为患者提供更多选择。
Lp(a)是动脉粥样硬化的独立危险因素,即使LDL-C控制良好,Lp(a)升高仍可能增加心血管事件风险。因此,综合管理Lp(a)和LDL-C至关重要。虽然Lp(a)尚无特效药,但通过强化LDL-C控制和脂蛋白血浆置换,患者仍能有效降低心血管风险。
参考文献:
【1】2025 AACE Guidelines for Dyslipidemia
【2】Schwartz GG, et al. Alirocumab and Cardiovascular Outcomes after Acute Coronary Syndrome. N Engl J Med. 2018; 379(22): 2097-2107



 微信扫一扫打赏
微信扫一扫打赏 支付宝扫一扫打赏
支付宝扫一扫打赏



评论列表()